Клиническое выздоровление. Применение метронидазола, тинидазола, ниморазола, тенонитрозола, орнидазола в лечении больных с хроническим урогенитальным трихомониазом. Результаты исследований и их обсуждение
В основе выздоровления лежит потенцирование саногенных механизмов, формирование эффективных адаптивных процессов и реакций, которые ликвидируют причину болезни и/или её патогенные последствия, полностью восстанавливают гомеостаз организма. Такое выздоровление называют полным.
Полное выздоровление, однако, не означает возврата организма к его состоянию до болезни. Выздоровевший после болезни организм характеризуется качественно (и часто количественно) иными показателями жизнедеятельности: в нём формируются новые функциональные системы, меняется активность системы иммунобиологического надзора (ИБН), метаболизма, развиваются многие другие адаптивные изменения.
Выздоровление неполное
При сохранении в организме так называемых остаточных явлений болезни, отдельных структурных и функциональных отклонений от нормы после её завершения выздоровление называют неполным.
Рецидив
Рецидив – повторное развитие или повторное усиление (усугубление) симптомов болезни после их устранения или ослабления. Как правило, симптомы рецидива сходны с симптомами первичной болезни, хотя в некоторых случаях могут отличаться (например, при рецидиве хронического миелолейкоза могут доминировать признаки анемии).
Рецидивирование обычно является результатом действия причины, вызвавшей и первый эпизод болезни, снижения эффективности механизмов адаптации и/или резистентности организма к определённым факторам (например, снижение противоопухолевой резистентности организма может способствовать рецидивированию новообразований; подавление активности системы ИБН нередко сочетается с рецидивированием инфБ).
Ремиссия
Ремиссия – временное ослабление (неполная ремиссия) или устранение (полная ремиссия) признаков болезни. При некоторых заболеваниях ремиссия является их закономерным преходящим этапом (например, при малярии, ревматических болезнях, возвратном тифе), сменяющимся рецидивом. В этом случае ремиссия не означает выздоровления.
Наиболее часто ремиссии являются следствием либо своеобразия причины болезни (например, особенностей жизненного цикла малярийного плазмодия и возбудителя возвратного тифа), либо изменения реактивности организма (например, периодические сезонные ремиссии у больных с различными проявлениями герпетической инфекции), либо лечения пациента, не приводящего к полному выздоровлению (например, при терапии больных со злокачественными новообразованиями или ревматическими болезнями).
Осложнения
Осложнение –патологический процесс, состояние или реакция, развивающиеся на фоне основной болезни, но не обязательные для неё. Осложнения в большинстве случаев являются результатом опосредованного действия причины болезни либо её патогенетических звеньев (например, гипертонический криз при гипертонической болезни; ангиопатии и/или коматозные состояния при сахарном диабете; перфорация стенок желудка или кишечника при язвенной болезни). Осложнения усугубляют течение основной болезни.
При неблагоприятном развитии болезни возможны и другие исходы: затяжное, хроническое течение и прекращение жизнедеятельности, смерть пациента.
Смерть
Смерть – процесс прекращения жизнедеятельности организма. Этому предшествует более или менее длительный период умирания организма. Он включает: – преагонию, – терминальную паузу, – агонию, – клиническую смерть, – биологическую смерть. Первые четыре этапа периода умирания обратимы при условии своевременно и эффективно проводимых врачебных мероприятиях по реанимации организма. Биологическая смерть необратима.
Клиническая смерть – принципиально обратимый этап терминального состояния. Он характеризуется прекращением дыхания, сердцебиения и кровообращения. При нормотермии организма этот период длится обычно 3-6 минут, при гипотермии может быть пролонгирован до 15-25 минут. Основным фактором, определяющим длительность периода клинической смерти, является степень гипоксии нейронов коры головного мозга.
На этапе клинической смерти необходимо проведение реанимационных мероприятий . К числу основных среди них относят: – возобновление дыхания (искусственная вентиляция легких); –восстановление сердечной деятельности и кровообращения (массаж сердца, при необходимости – его дефибрилляция, искусственное кровообращение с использованием оксигенированной крови); –коррекция кислотно-основного состояния (устранение ацидоза) и ионного баланса; – нормализация состояния системы гемостаза и микрогемоциркуляции. Успех указанных мероприятий повышается при их проведении в условиях гипотермии и/или гипербарической оксигенации.
Оживленный организм в течение более или менее длительного времени находится в особом нестабильном – постреанимационном патологическом состоянии. Онополучило название «постреанимационная болезнь». Это состояние, как правило, включает несколько стадий: –временной стабилизации жизнедеятельности организма, – преходящей дестабилизации ее (в связи с развитием разной степени выраженности полиорганной недостаточности), – нормализации жизнедеятельности и выздоровления пациента.
Биологическая смерть – необратимое прекращение жизнедеятельности организма и физиологических процессов в нем. При этом оживление организма как целостной системы (включая и восстановление мышления) уже невозможно, хотя еще и есть возможность возобновить функцию отдельных органов (сердца, почек, печени и др.).
Исследования, проведенные с помощью современной медицинской техники, показали, что нормализация структуры пораженного органа отстает во времени от вполне удовлетворительного самочувствия больного (заживление переломов костей и язвы желудка, рассасывание эксудата при пневмонии, полная организация очага некроза в мышце и т.д.).
Очень часто при вполне благополучном субъективном состоянии при обследовании выявляются незарубцевавшиеся язвы и т.д. Должно пройти много месяцев, чтобы после устранения врожденного или приобретенного порока сердца гипертрофия миокарда подверглась "обратному развитию", и сердце приняло размеры, близкие к исходным.
Быстрое восстановление функций происходит, как правило, за счет внутриклеточных регенераторных процессов. Быстро спадающий отек ткани снижает болевые ощущения, а для "обратного развития" структурных изменений паренхимы органов и,особенно, склеротических изменений требуется более длительное время. Следует также помнить, что современная лекарственная терапия оказывает влияние прежде всего на снятие отека, интоксикации, снижение температуры тела и другие симптомы, а оказать столь быстрое влияние на структурные изменения она не может. Следовательно, происходит увеличение временного разрыва между клиническим выздоровлением и возвращением структурных изменений к состоянию, бывшему до болезни.
Благодаря электронной микроскопии удалось выяснить, что на субклеточном уровне (митохондрии и другие клеточные органоиды) достаточно долго сохраняются морфологический атипизм и "ненормальности" строения, то есть не происходит полный возврат к исходным ультраструктурам.
Восстановление функций организма происходит быстрее, и общее самочувствие становится вполне нормальным у больного, но полного восстановления структуры органов еще долго нет. Таким образом, следует отметить, что любая болезнь имеет бессимптомный период в начале болезни, во время которого структурные изменения опережают клинические проявления, а также такой же период в конце заболевания, когда структурные изменения еще остаются при вполне благополучном самочувствии больного. Можно образно представить себе, что надводная часть айсберга - это клиническая картина болезни, а его подводная (большая часть) - это полный объем изменений, происходящих в организме на биохимическом, клеточном, тканевом и органном уровнях организации человека.
Из этого понимания течения болезни можно сделать несколько важных выводов.
1. Не существует функциональных нарушений без соответствующих структурных изменений.
2. Клинические проявления болезни при достаточно хороших компенсаторно-приспособительных реакциях организма имеют место чаще всего при их срыве из-за значительных структурных изменений.
3. Важную роль в раннем выявлении заболеваний играют функциональные нагрузки, позволяющие обнаружить еще скрытую структурнофункциональную недостаточность того или иного органа или висцеральной системы. Кроме этого имеется ряд методов (молекулярно-генетическая диагностика, бактериологические и вирусологические методы и др.), которые позволяют проводить раннюю диагностику.
4. Болезнь может существовать длительное время, но не сопровождаться "нарушением здоровья" и "утратой трудоспособности".
Catad_tema Мочеполовые инфекции - статьи
Применение метронидазола, тинидазола, ниморазола, тенонитрозола, орнидазола в лечении больных с хроническим урогенитальным трихомониазом
В.М. Kрасовский
Институт урологии АМН Украины (Kиев)
Изучена сравнительная эффективность использования препаратов Метронидазола, Тинидазола, Ниморазола, Тенонитрозола, Орнидазола в лечении 126 больных урогенитальным трихомониазом. Эффективность Метронидазола составила 40,4%, Тинидазола – 44,1%, Ниморазола – 85,7%, Тенонитрозола – 89,7%, Орнидазола – 93,3%, Орнидазола + Тенонитрозола – 97,7%. Препараты отличаются различной переносимостью и количеством побочных эффектов: Метронидазол – 23,3%, Тинидазол – 25%, Нимора-зол – 12,5%, Тенонитрозол – 12%, Орнидазол – 9,1%, Орнидазол + Тенонитрозол – 9,1%. Лучшие результаты получены в группах пациентов, которые получали: Орнидазол (93,3%), Тенонитрозол (89,7%), а также комбинация их последовательного применения Орнидазол + Тенонитрозол (97,7%). Результаты исследования можно использовать в клинической практике.
Kлючевые слова: хронический урогенитальный трихомониаз, лечение, Метронидазол, Тинидазол, Ниморазол, Тенонитрозол, Орнидазол.
Research of comparative efficiency of application of metronidazolum, tinidazolum, nimorazolum, tenonitrazolum, ornidazolum in treatment of patients with chronic urogenital trichmoniasis. V.M. Krasovsky
The comparative is studied efficiency of the use of preparations of Metronidazolum, Tinidazolum, Nimorazolum, Tenonitrazolum, Ornidazolum in treatment of patients with chronic urogenital trichmoniasis for 126 patients. Efficiency of Metronidazolum was 40,4%, Tinidazolum – 44,1%, Nimorazolum - 85,7%, Tenonitrazolum - 89,7%, Ornidazolum - 93,3%, Ornidazolum + Tenonitrazolum - 97,7%. Preparations differ different bearableness and amount of side effects: Metronidazolum - 23,3%, Tinidazolum - 25%, Nimorazolum - 12,5%, Tenonitrazolum - 12%, Ornidazolum - 9,1%, Ornidazolum + Tenonitrazolum - 9,1%. The best results are got in groups which got: Ornidazolum (93,3%), Tenonitrazolum (89,7%), and also combi nation of their successive application of Ornidazolum + Tenonitrazolum (97,7%). Research results can be recommended for the use in clinical practice.
Keywords: chronic urogenital trichmoniasis, treatment, Metronidazolum, Tinidazolum, Nimorazolum, Tenonitrazolum, Ornidazolum.
В последние десятилетия трихомониаз получил широкое распространение. Чаще всего это заболевание диагностируют у мужчин и женщин молодого возраста – от 16 до 35 лет, из которых большой процент больных составляют лица с другими венерическими заболеваниями и те, кто часто меняют половых партнеров .
Заражение трихомониазом происходит в основном половым путем, бытовым путем (плавая в бассейне или реке, в душе, в сауне) заразиться практически невозможно. Однако в сперме, моче и воде возбудитель остается жизнеспособным в течение 24 ч. У больных или у тех, кто перенес эту инфекцию, вырабатываются сывороточные и секреторные антитела, которые указывают на возбудителя, но иммунитет в отношении трихомонадной инфекции не развивается .
К главным особенностям заболевания следует отнести то, что возбудитель очень легко передается человеку, имевшему половую связь с инфицированным; наличие на поверхности микроорганизмов гиалуронидазы, каталазы, амилазы; способность повторять рельеф эпителиальной клетки и проникать в клетку хозяина; способность защититься от разрушительного действия организма с помощью фиксации на своей поверхности антитрипсина; наличие прямой зависимости вирулентности урогенитальных трихомонад от их гемолитической активности; способность прикрепляться к лейкоцитам, эритроцитам, эпителиальным клеткам за счет гликопротеида.
Выделяют несколько форм трихомониаза: свежая острая, подострая, торпидная; хроническая; трихомонадоносительство. Хроническая форма заболевания характеризуется малосимптомным течением, когда с момента заражения прошло более 2 мес. Периодические обострения могут быть спровоцированы снижением сопротивляемости организма, чрезмерным употреблением алкоголя, изменением рН содержимого мочеиспускательного канала. Трихомонадоносительство – форма заболевания, при которой отсутствуют какие-либо симптомы .
Трихомониаз – многоочаговое заболевание. По данным Всемирной организации здравоохранения (1995), только у 10,5% больных трихомониаз протекает как моноинфекция, в 89,5% случаев выявляются смешанные трихомонадные инфекции в различных комбинациях: с микоплазмами – 47,3%; с гонококками – 29,1%; с гарднереллой – 31,4%; с уреаплазмой – 20,9%; с хламидиями – 20%; с грибами – 15%.
Диагностика трихомониаза осуществляется на основании клинических признаков и результатов лабораторных исследований. Для получения более точного результата используют сразу несколько методов, а материал для изучения берут из различных очагов воспаления. Применяют следующие лабораторные методы: латекс-агглютинация (используют для выявления трихомонадоносительства); культуральные (используют для диагностики атипичных форм); иммунологические; микроскопия нативного препарата (позволяет по грушевидной или овальной форме, а также характерным движениям микроорганизма определить наличие трихомонады); микроскопия окрашенного препарата (дает возможность проводить исследования, когда материал взят достаточно давно); люминесцентная микроскопия (основан на свечении микроорганизма в ультрафиолетовых лучах). Самый точный и современный метод – ДНK (ПЦР)-диагностика. Для ее проведения из биологического материала извлекают генетически уникальный кусочек ДНK микроорганизма. Все возможные ошибки данного метода составляют 5%. Этот метод отличается не только точностью, но и скоростью выполнения (1–2 дня) .
Лечение трихомониаза назначают обязательно после осмотра и лабораторного обследования с учетом количества очагов инфекции, тяжести заболевания и индивидуальных особенностей пациента. Кроме того, лечение трихомониаза по требованиям ВОЗ проводят всем половым партнерам, если у одного из них обнаружена инфекция (трихомонада). Особенностью заболевания является наличие множества очагов инфекции. Учитывая этот факт, больным назначают комплексную терапию, включающую: прротивопротозойные препараты; антибактериальные препараты; местное лечение; этиотропные методы; витамины; биостимуляторы; иммунокоррегирующие методы; симптоматическое лечение; гепатопротекторы; противогрибковые препараты. На фоне лечения половая жизнь и прием алкоголя не рекомендуются . Выбор тактики лечения следует осуществлять индивидуально, с учетом клинико-анамнестических данных.
Лечение острой формы: этиотропная терапия; антибактериальные препараты по индивидуальным показаниям; ферменты, улучшающие пищеварение; витаминотерапия; противотрихомонадные препараты для местного применения в очагах воспаления. По окончании этиотропной терапии рекомендуется провести курс антиоксидантной терапии (перорально и местно) в сочетании с гепатопротекторными средствами.
Лечение хронической формы:
- Подготовительный этап: лекарственные средства, повышающие общий и/или местный иммунитет (по показаниям); витаминотерапия; антиоксиданты; местное лечение очагов поражения.
- Базисная терапия: противотрихомонадные препараты; антибактериальные препараты по показаниям; иммуномодулирующие препараты по показаниям; ферменты, улучшающие пищеварение; протеолитические ферменты; гормонзаместительные препараты (внутрь или местно) по показаниям; антиоксиданты.
- Восстановительная терапия: гепатопротекторы; антиоксиданты - местно; физиотерапевтические процедуры; витаминотерапия.
Первое контрольное обследование у мужчин проводят на 7–10-й день после окончания лечения трихомониаза: пальпаторное обследование предстательной железы и семенных пузырьков, микроскопическое исследование их секрета. Через 1 нед назначают провокацию. Если после провокации трихомонадная инфекция не обнаружена, то на последнее контрольное обследование пациент приходит через 1 мес.
Kритерии излеченности
Различают этиологическое и клиническое выздоровление от трихомониаза. Этиологическое выздоровление: при контрольных обследованиях после курса лечения трихомонады не обнаружены в течение 1–2 мес. у мужчин. Для контрольных обследований применяют культуральные и бактериоскопические лабораторные методы. Kлиническое выздоровление: исчезновение симптомов болезни. Нередко у мужчин после наступления этиологического выздоровления симптомы трихомониаза сохраняются. Посттрихомонадные воспалительные процессы бывают у пациентов с осложненными или хроническими формами болезни .
Этиотропную терапию трихомониаза проводят несколькими препаратами: это метронидазол, тинидазол, ниморазол, тенонитрозол, орнидазол, секнидазол, флюнидазол, карнидазол. Первых пять препаратов зарегистрированы и их применяют в Украине.
Лекарственная резистентность, ее механизмы и клиническое значение
В последние годы у микроорганизмов все чаще вырабатывается лекарственная резистентность к различными препаратам в связи с неконтролируемым, недостаточно интенсивным или длительным лечением, самолечением. Частота развития резистентности и уровень устойчивости существенно различаются в зависимости от вида микроорганизма, химического состава препарата, эффективности применяемых доз и схем лечения.
Развитие устойчивости связано в первую очередь со снижением активности нитроредуктаз микробной клетки и соответственно со снижением внутриклеточной биотрансформации препаратов. В результате уменьшается образование комплексов с ДНK, снижаются процессы образования свободных радикалов и концентрация цитотоксических продуктов метаболизма. Развитие устойчивости может быть обусловлено также нарушением транспортных систем клетки (снижение проницаемости клеточной стенки у анаэробов и микроаэрофилов и клеточной оболочки у простейших), включая феномен выброса.
Kроме того, главной проблемой в лечении трихомониаза сегодня выступает всевозрастающая резистентность трихомонады к антипротозойным препаратам. Так, согласно исследованиям, проведенным авторами в 1999 г., всего 35% штаммов трихомонад чувствительны к метронидазолу . Согласно другим исследованиям, всего 55% трихомонад чувствительны к тинидазолу . Соответственно изучение изменяющейся чувствительности трихомонад к современным антипротозойным препаратам является актуальной проблемой лечения трихомониаза и микст-инфекций половых путей.
В связи с этим была сделана попытка провести исследование сравнительной эффективности различных противотрихомонадных препаратов.
МАТЕРИАЛЫ И МЕТОДЫ
В отделении сексопатологии и андрологии Института урологии АМН Украины изучали клиническую эффективность различных противотрихомонадных препаратов: Метронидазола, Тинидазола, Ниморазола, Тенонитрозола, Орнидазола у больных хроническим урогенитальным трихомониазом. Кроме того, проводили ретроспективный анализ чувствительности влагалищной трихомонады к различным противопротозойным препаратам и оценивали их эффективность и безопасность.
Под наблюдением находились 370 пациентов с хроническим урогенитальным трихомониазом в возрасте от 21 до 48 лет и длительностью заболевания от 3 мес. до 8 лет. Диагноз урогенитального трихомониаза устанавливали на основании общепринятых принципов с выявлением трихомонад, что подтверждено микроскопией окрашенных мазков, исследованием нативного препарата, культуральным методом, а также методом ПЦР.
Все больные были разделены на группы:
1-я группа (52 пациента) получала в качестве противотрихомонадного препарата Метронидазол в стандартной дозе на протяжении 10 дней.
2-я группа (43 пациента) – Тинидазол по 0,5 г 4 раза в день с интервалом 15 мин 2 дня.
3-я группа (49 мужчин) – Орнидазол по 0,5 г 2 раза в день на протяжении 10 дней.
4-я группа (56 мужчин) – Ниморазол по 0,5 г 2 раза в день на протяжении 6 дней.
5-я группа (126 мужчин) – Тенонитрозол по 0,25 г 2 раза в день на протяжении 8 дней.
6-я группа (44 мужчин) – Орнидазол по 0,5 г 2 раза в день на протяжении 10 дней и Тенонитрозол по 0,25 г 2 раза в день на протяжении 8 дней.
С целью коррекции иммунного статуса назначали индуктор интерферона растительного происхождения кагоцел; как гепатопротектор использовали препарат легалон – 140 мг в день стандартных доз на курс лечения. Для получения антибактериального эффекта (ввиду наличия TANK-функции у трихомонады) назначали препарат группы макролидов кларитромицин в дозе по 500 мг 2 раза в сутки на протяжении 10 дней; пациенты также получали симптоматическое и физиотерапевтическое лечение.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
Результаты комплексного курсового лечения пациентов в номинации «клиническое выздоровление» через 30 дней после окончания лечения приведено в табл. 1.
Таблица 1. Эффективность этиотропной терапии урогенитального трихомониаза различными препаратами
| Клиническая группа | Препарат | Количество больных | Клиническое выздоровление (абс. число) | Клиническое выздоровление, % |
| 1-я | Метронидазол | 52 | 21 | 40,4 |
| 2-я | Тинидазол | 43 | 19 | 44,1 |
| 3-я | Орнидазол | 49 | 45 | 93,3 |
| 4-я | Ниморазол | 56 | 48 | 85,7 |
| 5-я | Тенонитрозол | 126 | 113 | 89,7 |
| 6-я | Орнидазол + Тенонитрозол | 44 | 43 | 97,7 |
Результаты микроскопии секрета предстательной железы и молекулярно-генетического исследования соскоба слизистой оболочки мочеиспускательного канала мужчин в динамике приведено в табл. 3.
Таблица 3. Результаты микроскопии секрета предстательной железы при этиотропной терапии урогенитального трихомониаза различными препаратами
| Клиническая группа | Препарат | Количество больных | Микроскопия секрета ПЖ | ПЦР |
| 1-я | Метронидазол | 52 | 18 (34,6%) | 21 (40,4%) |
| 2-я | Тинидазол | 43 | 16 (37,2%) | 19 (44,1%) |
| 3-я | Орнидазол | 49 | 44 (89,8) | 45 (93,3%) |
| 4-я | Ниморазол | 56 | 44 (78,5%) | 48 (85,7%) |
| 5-я | Тенонитрозол | 126 | 121 (88,0%) | 113 (89,7%) |
| 6-я | Орнидазол + Тенонитрозол | 44 | 43 (97,7%) | 43 (97,7%) |
Kак видно из приведенных данных, лучшие результаты получены при использовании метода ПЦР в группах пациентов, которые получали: Орнидазол (93,3%), Тенонитрозол (89,7%), а также их комбинацию последовательного применения Орнидазол + Тенонитрозол (97,7%). Метод микроскопии показал несколько худшие результаты по всем группам пациентов, что обусловлено субъективностью самого метода и свойством мимикрии трихомонады. Но эффективность лечения в тех же группах была выше.
При проведении ретроспективного анализа чувствительности влагалищной трихомонады к различным противопротозойным препаратам оценивали их эффективность. Был проведен анализ культуральных посевов трихомонад с подбором чувствительности к антипротозойным средствам у 243 пациентов, которую определяли по проценту выявления высокой чувствительности к препарату (чистая зона 20 мм и более вокруг диска или отсутствие возбудителя в чашке с препаратом). Высокой чувствительностью обладал препарат в случае наличия этих показателей в более чем 75% культуральных посевах, средний - от 50 до 75%, низкий - менее 50%. Результаты представлены на рис. 1.
Рис 1. Процент высокой чувствительности трихомонады к различным препаратам
Кроме того, нами была оценена эффективность лечения различными препаратами больных, основываясь на полной эрадикации возбудителя, на что указывает молекулярно-генетический метод. Данные приведены на рис. 2.
Рис. 2. Эффективность терапии трихомониаза различными препаратами

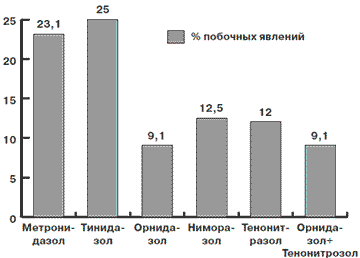
При определении количества побочных явлений при использовании различных противопротозойных препаратов выявлены результаты, которые приведены на рис. 3.
Рис. 3. Количество побочных явлений при использовании различных противопротозойных препаратов
ВЫВОДЫ
1. При изучении клинической эффективности различных противотрихомонадных препаратов у больных хроническим урогенитальным трихомониазом выявлено, что эффективность (по критерию эрадикации трихомонады) Метронидазола составила 40,4%, Тинидазола - 44,1%, Ниморазола -85,7%, Тенонитрозола - 89,7%, Орнидазола - 93,3%, Орнидазола + Тенонитрозола - 97,7%. ЛИТЕРАТУРА
2. Препараты отличаются различной переносимостью количеством побочных эффектов: Метронидазол - 23,3%, Тинидазол - 25%, Ниморазол - 12,5%, Тенонитрозол - 12%, Орнидазол - 9,1%, Орнидазол + Тенонитрозол - 9,1%.
3. Наиболее высокую чувствительность трихомонады выявили к препаратам Орнидазол (73,6%) и Атрикан (84,4%).
4. Лучшие результаты получены в группах пациентов, которые получали: Орнидазол (93,3%), Тенонитрозол (89,7%), а также комбинация их последовательного применения Орнидазол + Тенонитрозол (97,7%). Результаты исследования можно использовать в клинической практике.
1. Адаскевич В.П. Инфекции, передаваемые половым путем. Руководство для врачей. – М.: Медицинская книга, 1999. – 416 с.
2. Иванов О.Л., Ломоносов K.М., Алленов С.Н., Изюмова И.М. Опыт лечения острого трихомонадного уретрита // Российский журнал кожных и венерических болезней. – 1999. – № 3. – С. 57.
3. Ильин И.И. Негонококковые уретриты у мужчин. М.: Медицина, 1991. – 228 с.
4. Kлименко Б.В. Трихомониаз. М.: Медицина. – 1987. – 158 с.
5. Kривошеев Б.Н., Ермаков М.Н., Kриницына Ю.М. Тиберал в терапии урогенитального трихомоноза // Вести дерматол. венерол., 1997. – № 1. – С. 63–65.
6. Мавров И.И. Половые болезни. Руководство для врачей, интернов и студентов. Харьков: Факт. – 2002. – 789 с.
7. Молочков В.А. Урогенитальный трихомониаз и ассоциированные уретрогенные инфекции (эпидемиология, клиника, диагностика, лечение, профилактика). Российский журнал кожных и венерических болезней, 2000. – № 3. – С. 48–56.
8. Скрипкин Ю.K., Шарапова Г.Я., Селисский Г.Д. Болезни, передающиеся при половых контактах. М.: Медицина. – 1985. – 284 с.
9. Arroyo R., Gonzalez-Robles A., Martinez-Palomo A., Alderete J.F. (1993). Signalling of Trichomonas vaginalis for amoeboid transformation and adhesion synthesis follows cytoadherence. Mol. Microbiol., 7: 299–309.
10. Honigberg B. Trihomonads parasitic in humans. Springer – Verl, New York etc, 1990. – 424 p.
11. Kulda J., Vojtechovska M., Tachezy J. et al. Metronidazole resistance of Trichornonas vaginalis as a cause of treatment failure in trichomoni-asis. – A case report // Br. J. Vener. Dis. – 1982. – V. 58. – P. 394–399.
12. van Laarhoven P.H. Trichornonas vagi-nalis, a pathogen of prostatitis // Arch. Chir. Neerl. – 1967. – V. 19. – P. 263–273.
13. Saultz J.W., Toffler W.L. Trichornonas infections in men // Am. Fam. Physician. – 1989. – V. 39. – P. 177–180.
Б. однократное лабораторное обследования с отрицательным результатом, проведенное через 1-2 дня после окончания лечения
67. Пациент 18 лет, температура тела 39 0 С, стул слизистый, скудный с примесью зелени и крови. Живот запавший, болезненный при пальпации в левой подвздошной области, спазмированная сигмовидная кишка. Поставьте предварительный диагноз.
А. Иерсиниоз
Б. Ротавирусная инфекция
В. Шигеллез
Г. Сальмонеллез
68.Пациент Б., 24 лет, жалобы на повышение температуры до 40 0 С, головную боль, боли в мышцах, нечастый сухой кашель. Заболел остро, вчера. При осмотре: выражены симптомы интоксикации, заложенность носа, гиперемия дужек, миндалин. Со стороны легких и сердца без патологии. Наиболее оптимально назначение:
А. Интерферона α
Б. Озельтамивира
В. Ингавирина
Г. Ремантадина
69.У детей с ВИЧ-инфекцией ревакцинация против туберкулеза:
A. Проводится обязательно в декретированные сроки
Б. Не проводится
B. Проводится в зависимости от иммуннного статуса
Г. Проводится в зависимости от эпид. ситуации
70.Национальный календарь профилактических прививок по эпидемическим показаниям включает вакцинацию против:
A. Коклюша
Б. Чумы
Г. Вирусного гепатита С
71.Больной Л, 34 лет, госпитализирован в стационар на 14 день после покуса клеща с жалобами на головную боль, рвоту, лихорадку. При осмотре выявлены положительные менингеальные симптомы. Стандарт диагностики для установления этиологии заболевания будет включать:
A. Общий анализ крови, мочи, общий анализ ликвора
Б. Вирусологическое исследование ликвора, крови
B. Молекулярно-биологическое исследование крови
Г. Молекулярно-биологическое исследование ликвора, определение специфических антител в крови
72. Мужчина Л., 34 лет, охотник, был на охоте с 9 по 16 мая, 10 мая отмечен укус клеща, клещ удален. Привит против клещевого энцефалита 12 января и 1 мая текущего года. Обратился за помощью 17 мая. Меры профилактики клещевого вирусного энцефалита для него будут включать:
A. Экстренную пассивную специфическую профилактику (введение иммуноглобулина)
Б. Экстренную активную специфическую профилактику(введение 3-й дозы вакцины)
B. Неспецифическую профилактику
Г. Исследование клеща
73. Иммунитет после перенесенного клещевого энцефалита:
A. Нестойкий типоспецифический
Б. Стойкий пожизненный
B. До 6 мес.
Г. До 12 мес.
74. Больной У., 2 лет, болен 5 дней. Беспокоит лихорадка, сыпь, снижение аппетита. Страдает атопическим дерматитом. Мама накануне перенесла Herpeslabialis. Объективно: температура 38,9˚С, выражена интоксикация, распространенная полиморфная сыпь на коже (сгруппированные везикулы и пустулы, корочки, вторичные элементы (расчесы, лихенификация), беспокоит кожный зуд. Наиболее вероятный диагноз:
А. Ветряная оспа
Б. Атопический дерматит, осложненный вторичной бактериальной инфекцией
В. Стрептодермия
Г. Герпетиформная экзема Капоши
75.Вакциноассоциированный паралитический полиомиелит чаще встречается у:
A. Реципиентов живой полиомиелитной вакцины, контактных непривитых
Б. Контактных непривитых
B. Реципиентов инактивированной полиомиелитной вакцины
Г. Реципиентов живой полиомиелитной вакцины
76.Самым важным в лечении пациента с септическим шоком на фоне менингококковой инфекции является назначение:
A. Гормонов
Б. Антибиотиков
B. Инфузионной терапии
Г. Кислорода
77. В развитии септического шока при менингококковой инфекции участвуют:
A. Эндотоксин, цитокины, оксид азота
Б. Цитокины, экзотоксин, оксид азота
B. Иммуноглобулины, эндотоксин
Г. Все вышеперечисленное
78. У детей до года из менингеальных симптомов наиболее характерен симптом Лессажа. Это симптом:
А.Посадки (треножника)
Б. Подвешивания
A. Выбухания большого родничка
Г. Беспокойства на руках у мамы
79. Обследованию на малярию подлежат:
A. Лихорадящие больные с неустановленным диагнозом в течение 14 дней
Б.Лихорадящие больные с неустановленным диагнозом в течение 10 дней
Одной из характерных особенностей АД является клинический полиморфизм, определяющий разнообразие клинических форм заболевания. По мнению А.А. Антоньева и К.Н. Суворовой, АД характеризуется «двойной» клинической картиной (экзематизаци-ей и лихенификацией), в связи с чем и возникают определенные диагностические трудности.
Несмотря на существование до настоящего времени некоторых терминологических разногласий, обсуждение которых представлено в ряде отечественных монографий и на страницах научных журналов, исследователи единодушны в том, что АД начинается в раннем детском возрасте, имеет стадийность течения с возрастными особенностями клинических проявлений.
Официальной общепризнанной классификации АД не существует. На основе многолетних клинических наблюдений, изучения этиологии и имеющихся морфологических данных предлагается рабочая классификация АД у детей, в которой выделены стадии развития, фазы и периоды болезни, клинические формы в зависимости от возраста, распространенность кожного процесса, тяжесть течения, клинико-этиологические варианты (табл. 1).
Таблица 1. Рабочая классификация атопического дерматита у детей
| Категория классификации | Параметры классификации |
| Стадии развития, периоды и фазы болезни | 1. Начальная стадия. 2. Стадия выраженных изменений (период обострения): острая фаза, хроническая фаза. 3. Стадия ремиссии: неполная (подострый период), полная. 4. Клиническое выздоровление. |
| Клинические формы в зависимости от возраста | Младенческая, детская, подростковая |
| Распространенность | Ограниченный, распространенный, диффузный |
| Тяжесть течения | Легкое, средней тяжести, тяжелое течение |
| Клинико-этиологические варианты | С преобладанием пищевой, клещевой, грибковой, пыльцевой и прочих вариантов аллергии |
Согласно представленной классификации, выделяют следующие стадии развития АД: начальную, стадию выраженных изменений на коже, стадию ремиссии и клинического выздоровления.
Начальная стадия
. Развивается, как правило, у детей с экссудативно-катаральным типом конституции, характеризующимся наследственными, врожденными или приобретенными особенностями иммунологических, нейровегета-тивных и метаболических функций, определяющих предрасположенность организма к развитию аллергических реакций.
Наиболее ранними и частыми симптомами поражения кожи в начальной стадии
являются гиперемия и отечность кожи щек, сопровождающиеся легким шелушением. Вместе с этими симптомами могут наблюдаться гнейс (себорейные чешуйки вокруг большого родничка), «молочный струп» (ограниченное покраснение кожи лица и появление на ней корочек желтоватого цвета), преходящая эритема кожи щек, ягодиц. Особенностью начальной стадии заболевания является ее обратимость при условии своевременно начатого лечения с проведением соответствующих элиминационных мероприятий и назначением гипоаллергенной диеты. Именно на этой стадии болезни легче всего добиться обратного развития кожных высыпаний. Сохраняющееся среди педиатров мнение о том, что минимальные изменения на коже пройдут самостоятельно, без лечения, в корне ошибочно.
Стадия выраженных изменений, или период обострения.
Несвоевременное и неадекватное лечение кожных высыпаний (особенно у детей с неблагоприятным преморбидным фоном) приводит к переходу начальной стадии болезни в стадию выраженных изменений на коже, или период обострения (при рецидивах АД).
Клинические формы АД в этой стадии довольно разнообразны и зависят, главным образом, от возраста ребенка. В большинстве случаев дебют заболевания приходится на первый год жизни, однако оно может начаться в любом возрасте. При этом практически всегда период обострения АД проходит острую и хроническую фазы своего развития.
Острая фаза АД
характеризуется, главным образом, микровезикуляцией с развитием корок и появлением чешуек в следующей последовательности: эритема - папулы - везикулы - эрозии - корки - шелушение.
О хронической фазе АД
свидетельствует появление лихенификации, при которой последовательность кожных высыпаний можно представить следующим образом: папулы - шелушение - экскориации - лихенификация.
Стадия ремиссии
. В период ремиссии отмечается исчезновение или значительное уменьшение симптомов заболевания. Ремиссия может быть различной продолжительности - от нескольких недель и месяцев до 5 и более лет. В тяжелых случаях АД может протекать без ремиссии и рецидивировать всю жизнь.
Неполная ремиссия
- уменьшение или ослабление симптомов заболевания. Период неполной ремиссии некоторые авторы называют подострой фазой течения АД.
Полная ремиссия
- исчезновение всех клинических симптомов заболевания.
Клиническое выздоровление. Стадия заболевания, при которой отсутствуют клинические симптомы болезни в течение Ъ и более лет, в зависимости от тяжести течения АД.
Клинические формы АД в зависимости от возраста.
Выделяют младенческую (в возрасте от 2-3 месяцев до 3 лет), детскую (от 3 до 12 лет) и подростковую (от 12 до 18 лет) формы АД.
Младенческая форма (от 2-3 месяцев до 3 лет)
. Заболевание у детей данной возрастной группы имеет характерные признаки: кожа гиперемирована и отечна, покрыта микровезикулами. Наблюдаются экссудация (мокнутие), корки, шелушение, трещины. Поражаются отдельные участки тела. Излюбленная локализация - область лица, за исключением носогубного треугольника. Кожные высыпания могут распространяться на наружную поверхность верхних и нижних конечностей, локтевые и подколенные ямки, запястья, туловище, ягодицы. Субъективно беспокоит зуд кожных покровов различной интенсивности. Дермографизм красный или смешанный.
Детская форма (or 3 до 12 лет)
. В этом возрасте характерны гиперемия (эритема), отек кожи, лихенификация (утолщение и усиление кожного рисунка в результате постоянного расчесывания и растирания кожи). Наблюдаются папулы, бляшки, эрозии, экскориации, геморрагические корочки. Трещины особенно болезненны на ладонях, пальцах и подошвах. Кожные покровы сухие, покрыты большим количеством мелкопластинчатых и отрубевидных чешуек.
Кожные высыпания возникают преимущественно на сгибательных поверхностях конечностей, переднезаднебоковой поверхности шеи, локтевых и подколенных ямках, тыльной стороне кисти. Может наблюдаться гиперпигментация век в результате расчесывания глаз, появление характерной складки кожи под нижним веком (линия Денье-Моргана). Зуд различной интенсивности. Дермографизм белый или смешанный.
Подростковая форма (от 12 до 18 лет) . Характеризуется наличием крупных, слегка блестящих лихеноидных папул, выраженной лихени-фикацией, а также множеством экскориаций и геморрагических корочек в очагах поражения, которые локализуются на лице (периорбитальная, периоральная области), шее (в виде «декольте»), локтевых сгибах, вокруг запястий и на тыльной поверхности кистей. Зуд сильный. Отмечают нарушение сна, невротические реакции. Дермографизм белый, стойкий.
Распространенность кожного процесса . Распространенность кожного процесса оценивается по площади очагов поражения.
Степень тяжести
. При оценке степени тяжести АД в клинической практике учитываются интенсивность кожных высыпаний, распространенность процесса, размеры лимфатических узлов, частота обострений в течение года, продолжительность ремиссии.
Легкое течение АД
. Характеризуется высыпаниями, проявляющимися легкой гиперемией, экссудацией и шелушением, единичными папуло-везикулезными элементами, слабым зудом кожных покровов, увеличением лимфатических узлов до размеров горошины. Частота обострений - 1-2 раза в год. Продолжительность ремиссий - 6-8 месяцев.
АД средней тяжести
. Наблюдаются множественные очаги поражения на коже с достаточно выраженными экссудацией или инфильтрацией и лихенификацией, экскориациями и геморрагическими корками. Зуд умеренный или сильный. Лимфатические узлы увеличены до размеров лесного ореха или фасоли. Частота обострений 3-4 раза в год. Длительность ремиссий - 2-3 месяца.
Тяжелое течение АД
. Тяжелому течению АД свойственны множественные и обширные очаги поражения с выраженной экссудацией, стойкой инфильтрацией и лихенификацией, с глубокими линейными трещинами, эрозиями. Зуд сильный, «пульсирующий» или постоянный. Наблюдается увеличение практически всех групп лимфатических узлов до размеров лесного или грецкого ореха. Частота обострений - 5 и более раз в год. Ремиссия непродолжительная, от 1 до 1,5 месяцев, и, как правило, неполная. В крайне тяжелых случаях АД может протекать без ремиссий, с частыми обострениями.
Степень тяжести АД в европейских странах оценивается по шкале SCORAD (Scoring of Atopic Dermatitis), которая разработана Европейской рабочей группой. По мнению большинства исследователей, она позволяет объективно оценить степень тяжести АД . Система SCORAD учитывает следующие показатели: (А) распространенность кожного процесса, (В) интенсивность клинических проявлений и (С) субъективные симптомы (Подродное описание системы SCORAD можно найти на сайте в разделе Методические пособия - Прим. ред. ).
Пищевая аллергия
. АД характеризуется возникновением кожных симптомов после употребления пищевых продуктов, к которым повышена чувствительность (коровье молоко, злаки, яйцо, морепродукты, овощи и фрукты яркой красной или оранжевой окраски и т. д.). Положительная клиническая динамика наблюдается, как правило, при назначении элиминацион-ной диеты.
Клещевая сенсибилизация
. АД характеризуется тяжелым, непрерывно рецидивирующим течением, круглогодичными обострениями и усилением зуда кожных покровов в ночное время. Улучшение состояния наблюдается при прекращении контакта с клещами домашней пыли: смене места жительства, госпитализации. Элиминационная диета не дает выраженного эффекта.
Грибковая сенсибилизация
. Обострения АД связаны с приемом пищевых продуктов, обсемененных спорами грибов Alternaria, Aspergillus, Mucor, Candida, или продуктов, в процессе изготовления которых используются плесневые грибы. Обострению также способствуют сырость, наличие плесени в жилых помещениях, назначение антибиотиков (особенно антибиотиков пенициллинового ряда). Для грибковой сенсибилизации характерно тяжелое течение болезни с возникновением обострений осенью и зимой.
Пыльцевая сенсибилизация
. Обострение АД, обусловленного пыльцевой сенсибилизацией, возникает в разгар цветения деревьев, злаковых или сорных трав. У этих больных обострение заболевания может возникать также в связи с употреблением пищевых аллергенов, имеющих общие антигенные детерминанты с пыльцой деревьев (орехи, яблоки, баютажаны, абрикосы, персики и другие продукты растительного происхождения). Как правило, сезонные обострения АД сочетаются с классическими проявлениями поллиноза (риноконъюнктивальный синдром, ларинготрахеит, обострения бронхиальной астмы), однако в ряде случаев могут протекать изолированно.
Эпидермальная сенсибилизация
. Заболевание обостряется при контакте ребенка с домашними животными или изделиями из шерсти животных. При эпидермальной аллергии АД нередко сочетается с аллергическим ринитом.
Следует учитывать, что «чистые» варианты грибковой, клещевой и пыльцевой сенсибилизации встречаются редко. Обычно речь идет о преобладающей роли того или иного вида аллергена.
Надеемся, что предложенная рабочая классификация АД поможет практическим врачам правильно поставить диагноз и на его основе выбрать соответствующую терапевтическую тактику ведения больного.
Материалы для данной главы предоставили: Гребенюк В.Н., Казначеева Л.Ф., Коростовцев Д.С., Короткий Н.Г., Огородова Л.М., Ревякина В.А., Синявская О.А., Торопова Н.П.
